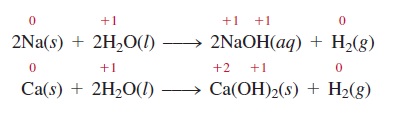Reaksi asam-basa dapat dicirikan sebagai proses transfer proton, sedangkan golongan reaksi yang disebut oksidasi-reduksi, atau reaksi redoks, reaksi ini dianggap sebagai reaksi transfer-elektron. Reaksi reduksi oksidasi sangat banyak menjadi bagian dari dunia di sekitar kita. Mulai dari pembakaran bahan bakar fosil hingga aksi pemutih rumah tangga. Selain itu, sebagian besar unsur logam dan nonlogam diperoleh dari bijihnya dengan proses oksidasi atau reduksi.
Banyak reaksi redoks terjadi di dalam air, tetapi tidak semua reaksi redoks terjadi dalam larutan berair. Kita memulai diskusi dengan reaksi dua unsur yang bergabung membentuk senyawa. Perhatikan pembentukan senyawa magnesium oksida (MgO) dari magnesium dan oksigen (Gambar 4.9):
2Mg(s) + O₂(g) → 2MgO(s)

Gambar 4.9 Magnesium dibakar dengan oksigen membentuk magnesium oksida
Magnesium oksida (MgO) adalah senyawa ionik yang tersusun dari ion Mg²⁺ dan O²⁻. Dalam reaksi ini, dua atom Mg melepaskan atau mentransfer empat elektron kepada dua atom O (dalam O₂). Untuk memudahkan, kita dapat menganggap proses ini sebagai dua langkah terpisah, pertama melibatkan lepasnya empat elektron dari dua atom Mg dan selanjutnya adalah penerimaan empat elektron oleh molekul O₂:
2Mg → 2Mg²⁺ + 4e⁻
O₂ + 4e⁻ → 2O²⁻
Masing-masing langkah ini disebut setengah reaksi, yang secara eksplisit menunjukkan elektron yang terlibat dalam reaksi redoks. Jumlah dari setengah reaksi memberikan reaksi keseluruhan:
2Mg + O₂ + 4e⁻ → 2Mg²⁺ + 2O²⁻ + 4e⁻
atau, jika kita menghilangkan elektron yang muncul di kedua sisi persamaan,
2Mg + O₂ → 2Mg²⁺ + 2O²⁻
Akhirnya, ion Mg²⁺ dan O²⁻ bergabung membentuk MgO:
2Mg²⁺ + 2O²⁻ → 2MgO.
Istilah reaksi oksidasi mengacu pada setengah reaksi yang melibatkan lepasnya elektron. Kimiawan awalnya menggunakan "oksidasi" untuk menunjukkan kombinasi unsur dengan oksigen. Namun, sekarang memiliki makna yang lebih luas yang mencakup reaksi yang tidak melibatkan oksigen. Reaksi reduksi adalah setengah reaksi yang melibatkan penambahan elektron. Dalam pembentukan magnesium oksida, magnesium dioksidasi. Magnesium dikatakan bertindak sebagai agen pereduksi (reduktor) karena menyumbangkan elektron ke oksigen dan menyebabkan oksigen direduksi. Oksigen direduksi dan bertindak sebagai agen pengoksidasi (oksidator) karena oksigen menerima elektron dari magnesium, menyebabkan magnesium teroksidasi. Perhatikan bahwa tingkat oksidasi dalam reaksi redoks harus sama dengan tingkat reduksi; yaitu, jumlah elektron yang dilepas oleh zat pereduksi harus sama dengan jumlah elektron yang diterima oleh zat pengoksidasi.
Terjadinya transfer elektron lebih jelas dalam beberapa reaksi redoks daripada yang lain. Ketika seng logam ditambahkan ke dalam larutan yang mengandung tembaga (II) sulfat (CuSO₄), seng mereduksi Cu²⁺ dengan menyumbangkan dua elektron ke dalamnya:
Zn(s) + CuSO₄(aq) → ZnSO₄(aq) + Cu(s)
Dalam prosesnya, larutannya kehilangan warna biru yang menjadi ciri keberadaan ion Cu²⁺ terhidrasi (Gambar 4.10):
Zn(s) + Cu²⁺(aq) → Zn²⁺(aq) + Cu(s)
Setengah reaksi oksidasi dan reduksinya adalah
Zn → Zn²⁺ + 2e⁻
Cu²⁺ + 2e⁻ → Cu
Demikian pula, logam tembaga mereduksi ion perak dalam larutan perak nitrat (AgNO₃):
Cu(s) + 2AgNO₃(aq) → Cu(NO₃)₂(aq) + 2Ag(s)
atau
Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
Bilangan Oksidasi (Biloks)
Definisi reduksi dan oksidasi dalam hal melepas dan menerima elektron berlaku untuk pembentukan senyawa ionik seperti MgO dan reduksi ion Cu²⁺ oleh Zn. Namun, definisi ini tidak secara akurat mengkarakterisasi pembentukan hidrogen klorida (HCl) dan belerang dioksida (SO₂):
H₂(g) + Cl₂(g) → 2HCl(g)
S(s) + O₂(g) → SO₂(g)
Karena HCl dan SO₂ bukan senyawa ionik tetapi molekul, tidak ada elektron yang benar-benar ditransfer dalam pembentukan senyawa ini, seperti pada MgO. Namun demikian, para ahli kimia menemukan bahwa reaksi ini adalah reaksi redoks karena pengukuran secara eksperimen menunjukkan bahwa terdapat transfer sebagian elektron (dari H ke Cl dalam HCl dan dari S ke O dalam SO₂).
Untuk melacak elektron dalam reaksi redoks, penting untuk menetapkan bilangan oksidasi untuk reaktan dan produk. Bilangan oksidasi atom, juga disebut keadaan oksidasi, menandakan jumlah muatan yang dimiliki atom dalam molekul (atau senyawa ionik) jika elektron ditransfer sepenuhnya. Sebagai contoh, kita dapat menulis ulang persamaan sebelumnya untuk pembentukan HCl dan SO₂ sebagai berikut:
Angka-angka di atas simbol unsur adalah bilangan oksidasi. Dalam kedua reaksi yang ditunjukkan, tidak ada muatan pada atom dalam molekul reaktan. Jadi, bilangan oksidasi molekul adalah nol. Untuk molekul produk, bagaimanapun, diasumsikan bahwa transfer elektron lengkap telah terjadi dan atom telah melepas atau menerima elektron. Bilangan oksidasi mencerminkan jumlah elektron yang "ditransfer".
Gambar 4.10 Reaksi perpindahan logam dalam larutan. (a) Gelas pertama: Sebuah seng ditempatkan dalam larutan CuSO₄ biru. Segera ion Cu²⁺ direduksi menjadi logam Cu dalam bentuk lapisan gelap. Gelas kedua: Pada waktunya, sebagian besar ion Cu²⁺ direduksi dan larutan menjadi tidak berwarna. (b) Gelas pertama: Sepotong kawat Cu ditempatkan dalam larutan AgNO₃ yang tidak berwarna. Ion Ag⁺ direduksi menjadi logam Ag. Gelas kedua: Seiring berjalannya waktu, sebagian besar ion Ag⁺ direduksi dan larutan memperoleh warna biru yang khas karena adanya ion Cu²⁺ terhidrasi.
Bilangan oksidasi memungkinkan kita untuk mengidentifikasi unsur yang teroksidasi dan direduksi secara cepat. Unsur-unsur yang menunjukkan peningkatan bilangan oksidasi — hidrogen dan belerang dalam contoh-contoh sebelumnya — dioksidasi. Klorin dan oksigen direduksi, sehingga bilangan oksidasi menunjukkan penurunan dari nilai awalnya. Perhatikan bahwa jumlah bilangan oksidasi H dan Cl dalam HCl (+1 dan -1) adalah nol. Demikian juga, jika kita menambahkan muatan pada S (+4) dan dua atom O [2 x (2-)], totalnya adalah nol. Alasannya adalah bahwa molekul HCl dan SO₂ netral, sehingga muatan harus dihilangkan.
Kita menggunakan aturan berikut untuk menetapkan bilangan oksidasi:
- Dalam unsur bebas (yaitu, dalam keadaan tidak terkombinasi), setiap atom memiliki bilangan oksidasi nol. Jadi, setiap atom dalam H₂, Br₂, Na, Be, K, O₂, dan P₄ memiliki bilangan oksidasi yang sama: yaitu nol.
- Untuk ion yang hanya terdiri dari satu atom (yaitu, ion monatomik), bilangan oksidasi sama dengan muatan pada ion. Jadi, ion Li⁺ memiliki bilangan oksidasi +1; Ion Ba²⁺, +2; Ion Fe³⁺, +3; Ion I⁻, -1; Ion O²⁻, -2; dan seterusnya. Semua logam alkali memiliki bilangan oksidasi +1 dan semua logam alkali tanah memiliki bilangan oksidasi +2 dalam senyawanya. Aluminium memiliki bilangan oksidasi +3 dalam semua senyawanya.
- Bilangan oksidasi oksigen dalam sebagian besar senyawa (misalnya, MgO dan H₂O) adalah -2, tetapi dalam hidrogen peroksida (H₂O₂) dan ion peroksida (O₂²⁻), adalah -1.
- Bilangan oksidasi hidrogen adalah +1, kecuali ketika terikat pada logam dalam senyawa biner. Dalam kasus ini (misalnya, LiH, NaH, CaH₂), bilangan oksidasinya adalah -1.
- Fluorin memiliki bilangan oksidasi -1 dalam semua senyawanya. Halogen lain (Cl, Br, dan I) memiliki bilangan oksidasi negatif ketika mereka muncul sebagai ion halida dalam senyawanya. Ketika dikombinasikan dengan oksigen — misalnya dalam asam okso dan anion okso (lihat Bagian 2.7) —halida memiliki bilangan oksidasi positif.
- Dalam molekul netral, jumlah bilangan oksidasi semua atom harus nol. Dalam ion poliatomik, jumlah bilangan oksidasi semua unsur dalam ion harus sama dengan muatan bersih ion. Misalnya, dalam ion amonium (NH₄⁺) bilangan oksidasi N adalah -3 dan H adalah +1. Jadi jumlah bilangan oksidasi adalah -3 + 4 (+1) = +1, yang sama dengan muatan bersih dari ion.
- Bilangan oksidasi tidak harus bilangan bulat. Misalnya, bilangan oksidasi O dalam ion superoksida, O₂⁻, adalah -½.
Kita menerapkan aturan sebelumnya untuk menetapkan bilangan oksidasi dalam Contoh 4.4.
Contoh 4.4
Tetapkan bilangan oksidasi untuk semua unsur dalam senyawa dan ion berikut ini: (a) Li₂O, (b) HNO₃, (c) Cr₂O₇²⁻.
Strategi
Secara umum, kita mengikuti aturan yang baru saja dicatat untuk menetapkan bilangan oksidasi. Ingat bahwa semua logam alkali memiliki bilangan oksidasi +1, dan dalam banyak kasus hidrogen memiliki bilangan oksidasi +1 dan oksigen memiliki bilangan oksidasi -2 dalam senyawanya.
Penyelesaian
(a) Berdasarkan aturan 2 kita melihat bahwa litium memiliki bilangan oksidasi +1 (Li⁺) dan bilangan oksidasi oksigen adalah -2 (O²⁻).
(b) Ini adalah rumus untuk asam nitrat, yang menghasilkan ion H⁺ dan ion NO₃⁻ dalam larutan. Dari aturan 4 kita melihat bahwa H memiliki bilangan oksidasi +1. Dengan demikian gugus lain (ion nitrat) harus memiliki bilangan oksidasi bersih -1. Oksigen memiliki bilangan oksidasi -2, dan jika kita menggunakan x untuk mewakili bilangan oksidasi nitrogen, maka ion nitrat dapat ditulis sebagai
[N⁽ˣ⁾O₃⁽²⁻⁾]⁻
sehingga
x + 3(-2) = -1
atau
x = +5
(c) Dari aturan 6 kita melihat bahwa jumlah bilangan oksidasi dalam ion dikromat Cr₂O₇²⁻ harus -2. Kita tahu bahwa bilangan oksidasi O adalah -2, jadi yang tersisa hanyalah menentukan bilangan oksidasi Cr, yang kita misalkan disebut y. Ion dikromat dapat ditulis sebagai
sehingga
2(y) + 7(-2) = -2
atau
y = +6
Dalam setiap kasus, apakah jumlah bilangan oksidasi semua atom sama dengan muatan bersih pada spesi?
Tetapkan bilangan oksidasi untuk semua unsur dalam senyawa dan ion berikut ini: (a) PF₃, (b) MnO₄⁻.
Gambar 4.11 menunjukkan bilangan oksidasi yang diketahui dari unsur-unsur yang dikenal, diatur sesuai dengan posisinya di tabel periodik. Kita dapat meringkas isi gambar ini sebagai berikut:
- Unsur logam hanya memiliki bilangan oksidasi positif, sedangkan unsur bukan logam dapat memiliki bilangan oksidasi positif atau negatif.
- Bilangan oksidasi tertinggi yang dimiliki unsur dalam Golongan 1A-7A adalah nomor golongannya. Sebagai contoh, halogen berada di Golongan 7A, jadi bilangan oksidasi tertinggi yang mungkin adalah +7.
- Logam transisi (Golongan 1B, 3B-8B) biasanya memiliki beberapa kemungkinan bilangan oksidasi.
Gambar 4.11 Bilangan oksidasi unsur dalam senyawanya. Bilangan oksidasi yang lebih umum berwarna merah.
Jenis-jenis Reaksi Redoks
Di antara reaksi reduksi oksidasi yang paling umum adalah reaksi pembentukan (kombinasi), penguraian (dekomposisi), pembakaran, dan perpindahan (substitusi). Satu jenis yang juga terlibat disebut reaksi disproporsionasi, yang juga akan dibahas dalam bagian ini.
Reaksi Pembentukan (Kombinasi)
Reaksi pembentukan adalah reaksi di mana dua atau lebih zat bergabung membentuk produk tunggal. Gambar 4.12 menunjukkan beberapa reaksi kombinasi. Sebagai contoh,
Gambar 4.12 Beberapa reaksi redoks kombinasi sederhana. (a) Belerang terbakar di udara membentuk belerang dioksida. (b) Pembakaran natrium dalam klorin membentuk natrium klorida. (c) Aluminium bereaksi dengan bromin membentuk aluminium bromida.
Reaksi Penguraian (dekomposisi)
Reaksi penguraian adalah kebalikan dari reaksi pembentukan (kombinasi). Secara khusus, reaksi dekomposisi adalah penguraian senyawa menjadi dua atau lebih komponen (Gambar 4.13). Sebagai contoh,
Gambar 4.13 (a) Pada pemanasan, merkuri (II) oksida (HgO) terurai membentuk merkuri dan oksigen. (b) Pemanasan kalium klorat (KClO₃) menghasilkan oksigen, yang mendukung pembakaran bilah kayu.
Reaksi pembakaran
Reaksi pembakaran adalah reaksi di mana suatu zat bereaksi dengan oksigen, biasanya dengan melepaskan panas dan cahaya menghasilkan api. Reaksi antara magnesium dan sulfur dengan oksigen yang dijelaskan sebelumnya adalah reaksi pembakaran. Contoh lain adalah pembakaran propana (C₃H₈), komponen gas alam yang digunakan untuk pemanasan dan memasak rumah tangga:
C₃H₈(g) + 5O₂(g) → 3CO₂(g) + 4H₂O(l)
Pengaturan bilangan oksidasi atom C dalam senyawa organik lebih banyak terlibat. Di sini, kita hanya fokus pada bilangan oksidasi atom O, yang berubah dari 0 menjadi -2.
Reaksi Perpindahan (substitusi)
Dalam reaksi substitusi (perpindahan), ion (atau atom) dalam suatu senyawa digantikan oleh ion (atau atom) unsur lain: Sebagian besar reaksi perpindahan masuk ke dalam salah satu dari tiga subkategori: perpindahan hidrogen, perpindahan logam, atau perpindahan halogen.
1. Perpindahan Hidrogen.
Semua logam alkali dan beberapa logam alkali tanah (Ca, Sr, dan Ba), yang merupakan unsur logam paling reaktif, akan menggantikan hidrogen dari air dingin (Gambar 4.14):
Gambar 4.14 Reaksi (a) natrium (Na) dan (b) kalsium (Ca) dengan air dingin. Perhatikan bahwa reaksinya lebih kuat dengan Na daripada dengan Ca.
Banyak logam, termasuk yang tidak bereaksi dengan air, mampu menggantikan hidrogen dari asam. Misalnya, seng (Zn) dan magnesium (Mg) tidak bereaksi dengan air dingin tetapi bereaksi dengan asam klorida, sebagai berikut:
Gambar 4.15 menunjukkan reaksi antara asam klorida (HCl) dan besi (Fe), seng (Zn), dan magnesium (Mg). Reaksi-reaksi ini digunakan untuk menyiapkan gas hidrogen di laboratorium.
Gambar 4.15 Reaksi (a) besi (Fe), (b) seng (Zn), dan (c) magnesium (Mg) dengan asam hidroklorida membentuk gas hidrogen dan logam klorida (FeCl₂ ZnCl₂, MgCl₂). Reaktivitas logam-logam ini tercermin dalam laju pembentukan gas hidrogen, yang paling lambat untuk logam yang paling tidak reaktif, Fe, dan tercepat untuk logam yang paling reaktif, Mg.
2. Perpindahan Logam.
Suatu logam dalam suatu senyawa dapat digantikan oleh logam lain dalam keadaan unsur. Kita telah melihat contoh-contoh seng menggantikan ion tembaga dan tembaga menggantikan ion perak. Membalikkan peran logam tidak akan menghasilkan reaksi. Dengan demikian, logam tembaga tidak akan menggantikan ion seng dari seng sulfat, dan logam perak tidak akan menggantikan ion tembaga dari tembaga nitrat.
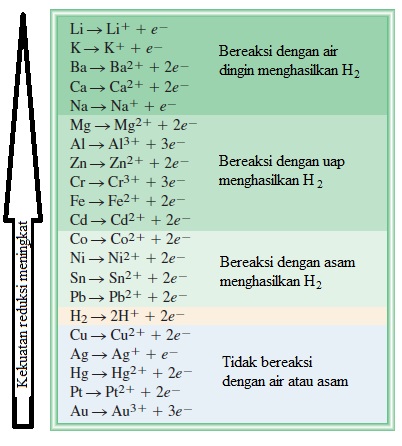
Cara mudah untuk memprediksi apakah reaksi substitusi logam atau hidrogen akan benar-benar terjadi adalah dengan merujuk pada seri aktivitas (kadang-kadang disebut seri elektrokimia), ditunjukkan pada Gambar 4.16. Pada dasarnya, seri aktivitas adalah ringkasan yang mudah dari hasil dari banyak kemungkinan reaksi perpindahan yang serupa dengan yang telah dibahas. Menurut seri ini, setiap logam di atas hidrogen akan memindahkannya dari air atau dari asam, tetapi logam di bawah hidrogen tidak akan bereaksi dengan air atau asam. Faktanya, setiap logam yang terdaftar dalam seri aktivitas akan bereaksi dengan logam apa saja (dalam senyawa) di bawahnya. Misalnya, Zn berada di atas Cu, sehingga logam seng akan menggantikan ion tembaga dari tembaga sulfat.
Gambar 4.16 Seri aktivitas untuk logam. Logam-logam tersebut diatur sesuai dengan kemampuannya untuk menggantikan hidrogen dari asam atau air. Li (litium) adalah logam yang paling reaktif, dan Au (emas) adalah yang paling tidak reaktif.
Reaksi substitusi logam menemukan banyak aplikasi dalam proses metalurgi, yang tujuannya adalah untuk memisahkan logam murni dari bijihnya. Sebagai contoh, vanadium diperoleh dengan memperlakukan vanadium (V) oksida dengan logam kalsium :
V₂O₅(s) + 5Ca(l) → 2V(l) + 5CaO(s)
Demikian pula, titanium diperoleh dari titanium (IV) klorida sesuai dengan reaksi
TiCl₄(g) + 2Mg(l) → Ti(s) + 2MgCl₂(l)
Dalam setiap kasus, logam yang bertindak sebagai zat pereduksi terletak di atas logam yang direduksi (yaitu, Ca di atas V dan Mg di atas Ti) dalam seri aktivitas. Kita akan melihat lebih banyak contoh dari jenis reaksi ini di Bab 19.
3. Substitusi Halogen.
Seri aktivitas lainnya yang merangkum perilaku halogen dalam reaksi perpindahan halogen:
F₂ > Cl₂ > Br₂ > I₂
Kekuatan unsur-unsur ini sebagai zat pengoksidasi berkurang jika kita mengurutkan Golongan 7A dari florin ke iodin, sehingga molekul florin dapat menggantikan ion klorida, bromida, dan iodida dalam larutan. Faktanya, molekul fluor sangat reaktif sehingga juga menyerang air; dengan demikian reaksi ini tidak dapat dilakukan dalam larutan berair. Di sisi lain, molekul klorin dapat menggantikan ion bromida dan iodida dalam larutan berair. Persamaan substitusi adalah
Persamaan ionik adalah
Molekul bromin, pada gilirannya, dapat menggantikan ion iodida dalam larutan:
Membalikkan peran halogen tidak menghasilkan reaksi. Dengan demikian, brom tidak dapat menggantikan ion klorida, dan yodium tidak dapat menggantikan ion bromida dan klorida.
Reaksi perpindahan halogen memiliki aplikasi industri langsung. Halogen sebagai suatu gugus adalah yang paling reaktif dari unsur-unsur bukan logam. Semua halogen adalah agen pengoksidasi kuat. Akibatnya, halogen ditemukan di alam dalam keadaan gabungan (dengan logam) sebagai halida dan tidak pernah sebagai unsur bebas. Dari keempat unsur ini, klorin sejauh ini merupakan bahan kimia industri yang paling penting. Pada tahun 2008 jumlah klorin yang diproduksi di Amerika Serikat adalah sekitar 25 miliar pound, menjadikan klorin sebagai bahan kimia industri peringkat kesepuluh. Produksi tahunan bromin hanya seperseratus dari klorin, sementara jumlah florin dan iodin yang dihasilkan bahkan lebih sedikit.
Memulihkan halogen dari halida mereka membutuhkan proses oksidasi, yang diwakili oleh
2X⁻ → X₂ + 2e⁻
di mana X menunjukkan unsur halogen. Air laut dan air asin alami (misalnya, air bawah tanah yang bersentuhan dengan endapan garam) adalah sumber yang kaya akan ion Cl₂, Br₂, dan I₂. Mineral seperti florit (CaF₂) dan kriolit (Na₃AlF₆) digunakan untuk membuat florin. Karena florin adalah zat pengoksidasi terkuat yang diketahui, tidak ada cara untuk mengubah ion F⁻ menjadi F₂ dengan cara kimia. Satu-satunya cara untuk melakukan oksidasi adalah dengan cara elektrolitik, yang rinciannya akan dibahas pada Bab 19. Secara industri, klorin, seperti florin, diproduksi secara elektrolitik.
Bromin dibuat secara industri dengan mengoksidasi ion Br₂ dengan klor, yang merupakan agen pengoksidasi yang cukup kuat untuk mengoksidasi ion Br₂ tetapi bukan air:
2Br⁻(aq) → Br₂(l) + 2e⁻
Salah satu sumber terkaya ion Br₂ adalah Laut Mati — sekitar 4000 bagian per juta (ppm) berdasarkan massa semua zat terlarut di Laut Mati adalah Br. Setelah oksidasi ion Br₂, brom dihilangkan dari larutan dengan meniupkan udara ke atas larutan, dan campuran udara-bromin kemudian didinginkan untuk memadatkan bromin (Gambar 4.17).
Yodium juga dibuat dari air laut dan air garam alami oleh oksidasi ion I₂ dengan klorin. Karena ion Br₂ dan I₂ selalu ada di sumber yang sama, keduanya teroksidasi oleh klorin. Namun, relatif mudah untuk memisahkan Br₂ dari I₂ karena yodium adalah padatan yang sedikit larut dalam air. Prosedur peniupan udara akan menghilangkan sebagian besar bromin yang terbentuk tetapi tidak akan memengaruhi kehadiran yodium.
Gambar 4.17 Pembuatan industri brom (cairan merah berasap) dengan mengoksidasi larutan berair yang mengandung ion Br₂ dengan gas klor.
Reaksi disproporsionasi
Jenis reaksi redoks yang khusus adalah reaksi disproporsionasi. Dalam reaksi disproporsionasi, suatu unsur dalam satu keadaan oksidasi secara bersamaan dioksidasi dan direduksi. Satu reaktan dalam reaksi disproporsionasi selalu mengandung unsur yang dapat memiliki setidaknya tiga keadaan oksidasi. Unsur itu sendiri dalam keadaan oksidasi menengah; yaitu, tingkat oksidasi yang lebih tinggi dan lebih rendah ada untuk unsur tersebut dalam produk. Dekomposisi hidrogen peroksida adalah contoh dari reaksi disproporsionasi:
Di sini bilangan oksidasi oksigen dalam reaktan (-1) meningkat menjadi nol pada O₂ dan menurun menjadi -2 pada H₂O. Contoh lain adalah reaksi antara molekul klorin dan larutan NaOH:
Reaksi ini menjelaskan pembentukan zat pemutih rumah tangga, karena ion hipoklorit (ClO₂) yang mengoksidasi zat pembawa warna dalam noda, mengubahnya menjadi senyawa tidak berwarna.
Akhirnya, menarik untuk membandingkan reaksi redoks dan reaksi asam-basa. Keduanya analog dengan reaksi asam-basa yang melibatkan transfer proton sedangkan reaksi redoks melibatkan transfer elektron. Namun, sementara reaksi asam basa cukup mudah dikenali (karena selalu melibatkan asam dan basa), tidak ada prosedur sederhana untuk mengidentifikasi proses redoks. Satu-satunya cara yang pasti adalah membandingkan bilangan oksidasi dari semua unsur dalam reaktan dan produk. Setiap perubahan dalam bilangan oksidasi menjamin bahwa reaksi tersebut bersifat redoks.
Klasifikasi berbagai jenis reaksi redoks diilustrasikan dalam Contoh 4.5.
Contoh 4.5
Klasifikasikan reaksi redoks berikut dan tunjukkan perubahan dalam bilangan oksidasi unsur:
(a) 2N₂O(g) → 2N₂(g) + O₂(g)
(b) 6Li(s) + N₂(g) → 2Li₃N(s)
(c) Ni(s) + Pb(NO₃)₂(aq) → Pb(s) + Ni(NO₃)₂(aq)
(d) 2NO₂(g) + H₂O(l) → HNO₂(aq) + HNO₃(aq)
Strategi
Tinjau definisi reaksi pembentukan, reaksi penguraian, reaksi pembakaran, reaksi perpindahan, dan reaksi disproporsionasi.
Penyelesaian
(a) Ini adalah reaksi penguraian karena satu reaktan diubah menjadi dua produk yang berbeda. Bilangan oksidasi N berubah dari +1 menjadi 0, sedangkan O berubah dari -2 menjadi 0.
(b) Ini adalah reaksi pembentukan (dua reaktan membentuk produk tunggal). Bilangan oksidasi Li berubah dari 0 menjadi +1 sedangkan N berubah dari 0 menjadi -3.
(c) Ini adalah reaksi perpindahan logam. Logam Ni menggantikan (mereduksi) ion Pb²⁺. Bilangan oksidasi Ni meningkat dari 0 menjadi +2 sedangkan Pb menurun dari +2 menjadi 0.
(d) Bilangan oksidasi N adalah +4 dalam NO₂ dan +3 dalam HNO₂ dan +5 dalam HNO₃. Karena bilangan oksidasi dari unsur yang sama meningkat dan menurun, ini adalah reaksi disproporsionasi.
Latihan
Identifikasi reaksi redoks berikut berdasarkan jenisnya:
(a) Fe + H₂SO₄ → FeSO₄ + H₂
(b) S + 3F₂ → SF₆
(c) 2CuCl → Cu + CuCl₂
(d) 2Ag + PtCl₂ → 2AgCl + Pt
Ulasan Konsep
Manakah dari reaksi pembentukan berikut ini yang bukan reaksi redoks?
(a) 2Mg(s) + O₂(g) → 2MgO(s)
(b) H₂(g) + F₂(g) → 2HF(g)
(c) NH₃(g) + HCl(g) → NH₄Cl(s)
(d) 2Na(s) + S(s) → Na₂S(s)