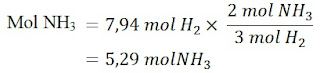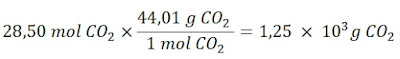Pertanyaan mendasar yang sering muncul di laboratorium kimia adalah "Berapa banyak produk yang akan dibentuk dari jumlah tertentu bahan awal (reaktan)?" Atau dalam beberapa kasus, kita mungkin mengajukan pertanyaan terbalik: "Berapa banyak bahan awal yang harus digunakan untuk mendapatkan jumlah produk tertentu? ”Untuk menginterpretasi suatu reaksi secara kuantitatif, kita perlu menerapkan pengetahuan kita tentang massa molar dan konsep mol. Stoikiometri adalah studi kuantitatif dari reaktan dan produk dalam reaksi kimia.
Meskipun satuan yang diberikan untuk reaktan (atau produk) adalah mol, gram, liter (untuk gas), atau beberapa satuan lainnya, kita menggunakan mol untuk menghitung jumlah produk yang terbentuk dalam suatu reaksi. Pendekatan ini disebut metode mol, yang berarti bahwa koefisien stoikiometri dalam persamaan kimia dapat diartikan sebagai jumlah mol dari setiap zat. Misalnya, amonia dalam industri disintesis dari hidrogen dan nitrogen sebagai berikut:
N₂(g)
+ 3H₂(g) → 2NH₃(g)
Koefisien stoikiometri menunjukkan bahwa satu molekul N₂ bereaksi dengan tiga molekul H₂ membentuk dua molekul NH₃. Oleh karena itu, jumlah mol relatif sama dengan jumlah molekul relatif:
N₂(g)
|
+ 3H₂(g)
|
→
|
2NH₃(g)
|
1 molekul
|
3 molekul
|
2 molekul
|
|
6,022 x 10²³ molekul
|
3(6,022 x 10²³ molekul)
|
3(6,022 x 10²³ molekul)
|
|
1 mol
|
1 mol
|
1 mol
|
Dengan demikian, persamaan ini juga dapat dibaca sebagai "1 mol gas N₂ bereaksi dengan 3 mol gas H₂ menghasilkan 2 mol gas NH₃." Dalam perhitungan stoikiometri, kita mengatakan bahwa tiga mol H₂ setara dengan dua mol NH₃, ditulis
3 mol H₂ ≃ 2 mol NH₃
di mana simbol ≃ berarti "setara stoikiometrik" atau "setara". Hubungan ini memungkinkan kita untuk menulis faktor konversi
Demikian pula, kita memiliki 1 mol N₂ ≃ 2 mol NH₃ dan 1 mol N₂ ≃ 3 mol H₂.
Mari kita perhatikan contoh sederhana di mana 6,0 mol H₂ bereaksi sepenuhnya dengan N₂ membentuk NH₃. Untuk menghitung jumlah NH₃ yang dihasilkan dalam mol, kita menggunakan faktor konversi yang memiliki H₂ dalam penyebut dan menulis
Sekarang asumsikan 16,0 g H₂ bereaksi sepenuhnya dengan N₂ membentuk NH₃. Berapa gram NH₃ yang akan terbentuk? Untuk melakukan perhitungan ini, kita mencatat bahwa hubungan antara H₂ dan NH₃ adalah rasio mol dari persamaan setara. Jadi kita harus terlebih dahulu mengkonversi gram H₂ ke mol H₂, kemudian ke mol NH₃, dan akhirnya ke gram NH₃. Langkah-langkah konversi adalah
gram H₂ → mol H₂ → mol NH₃ → gram NH₃
Pertama, kita mengubah 16,0 g H₂ menjadi jumlah mol H₂, menggunakan massa molar H₂ sebagai faktor konversi:
Selanjutnya, kita menghitung jumlah mol NH₃ yang dihasilkan.
Akhirnya, kita menghitung massa NH₃ yang dihasilkan dalam gram menggunakan massa molar NH₃ sebagai faktor konversi
Ketiga perhitungan terpisah ini dapat digabungkan dalam satu langkah sebagai berikut:
Demikian pula, kita dapat menghitung massa dalam gram N₂ yang dikonsumsi dalam reaksi ini. Langkah-langkah konversi adalah
gram H₂ → mol H₂ → mol N₂ → gram N₂
Dengan menggunakan hubungan 1 mol N₂ ≃ 3 mol H₂, kita menulis
Pendekatan umum untuk memecahkan masalah stoikiometri dirangkum berikutnya.
- Tuliskan persamaan kimia yang setara untuk reaksi.
- Konversi jumlah reaktan yang diberikan (dalam satuan gram atau satuan lainnya) ke jumlah mol.
- Gunakan rasio mol dari persamaan setara untuk menghitung jumlah mol produk yang terbentuk.
- Konversi mol produk menjadi gram (atau satuan lainnya) produk.
Gambar 3.8 menunjukkan langkah-langkah ini. Kadang-kadang kita mungkin diminta untuk menghitung jumlah reaktan yang diperlukan untuk membentuk jumlah produk tertentu. Dalam kasus tersebut, kita dapat membalikkan langkah-langkah yang ditunjukkan pada Gambar 3.8.
Gambar 3.8 Prosedur untuk menghitung jumlah reaktan atau produk dalam reaksi menggunakan metode mol.
Contoh 3.13 dan 3.14 menggambarkan penerapan pendekatan ini.
Contoh 3.13
Makanan yang kita makan diuraikan atau dipecah di dalam tubuh kita untuk menyediakan energi yang kita perlukan bagi pertumbuhan dan melakukan berbagai fungsi tubuh. Persamaan umum keseluruhan untuk proses yang sangat kompleks ini menggambarkan penguraian glukosa (C₆H₁₂O₆) menjadi karbon dioksida (CO₂) dan air (H₂O):
C₆H₁₂O₆ + 6O₂ → 6CO₂ + 6H₂O
Jika 856 g C₆H₁₂O₆ dikonsumsi oleh seseorang selama periode tertentu, berapa massa CO₂ yang dihasilkan?
Strategi
Melihat persamaan setara, bagaimana kita membandingkan jumlah C₆H₁₂O₆ dan CO₂? Kita dapat membandingkannya berdasarkan rasio mol dari persamaan setara. Dimulai dengan gram C₆H₁₂O₆, bagaimana kita mengkonversi ke mol C₆H₁₂O₆? Setelah mol CO₂ ditentukan dengan menggunakan rasio mol dari persamaan setara, bagaimana kita mengkonversi ke gram CO₂?
Penyelesaian
Kita mengikuti langkah-langkah sebelumnya dan Gambar 3.8.
Langkah 1: Persamaan setara diberikan dalam soal.
Langkah 2: Untuk mengkonversi gram C₆H₁₂O₆ ke mol C₆H₁₂O₆, kita menuliskan
Langkah 3: Dari rasio mol, kita melihat bahwa 1 mol C₆H₁₂O₆ ≃ 6 mol CO₂. Oleh karena itu, jumlah mol CO₂ yang terbentuk adalah
Langkah 4: Akhirnya, jumlah gram CO₂ yang terbentuk diberikan oleh
Setelah beberapa latihan, kita dapat menggabungkan langkah-langkah konversi
gram C₆H₁₂O₆ → mol C₆H₁₂O₆ → mol CO₂ → gram CO₂
Apakah jawabannya tampak masuk akal? Apakah massa CO₂ yang dihasilkan lebih besar dari massa C₆H₁₂O₆ yang bereaksi, meskipun massa molar dari CO₂ jauh lebih sedikit daripada massa molar C₆H₁₂O₆? Berapa rasio mol antara CO₂ dan C₆H₁₂O₆?
Latihan
Metanol (CH₃OH) terbakar di udara sesuai dengan persamaan
Metanol (CH₃OH) terbakar di udara sesuai dengan persamaan
2CH₃OH + 3O₂ → 2CO₂ + 4H₂O
Jika 209 gram metanol digunakan dalam proses pembakaran, berapa massa H₂O yang dihasilkan?
Contoh 3.14
Semua logam alkali bereaksi dengan air menghasilkan gas hidrogen dan hidroksida logam alkali yang sesuai. Reaksi tipikal adalah antara litium dan air:
2Li(s) + 2H₂O(l) → 2LiOH(aq) + H₂(g)
Berapa gram Li yang diperlukan untuk menghasilkan 9,89 g H₂?
Strategi
Pertanyaannya meminta jumlah gram reaktan (Li) untuk membentuk jumlah tertentu dari produk (H₂). Oleh karena itu, kita perlu membalikkan langkah-langkah yang ditunjukkan pada Gambar 3.8. Dari persamaan yang kita lihat bahwa 2 mol Li ≃ 1 mol H₂.
Penyelesaian
Langkah-langkah konversi adalah
gram H₂ → mol H₂ → mol Li → gram Li
Menggabungkan langkah-langkah ini ke dalam satu persamaan, kita dapat menuliskan
Periksa
Ada sekitar 5 mol H₂ dalam 9,89 g H₂, jadi kita membutuhkan 10 mol Li. Dari perkiraan massa molar Li (7 g), apakah jawabannya tampak masuk akal?
Latihan
Reaksi antara nitrit oksida (NO) dan oksigen membentuk nitrogen dioksida (NO₂) adalah langkah kunci dalam pembentukan kabut fotokimia:
2NO(g) + O₂(g) → 2NO₂(g)
Berapa gram O₂ yang dibutuhkan untuk menghasilkan 2,21 g NO₂?