Zat biasanya diidentifikasi berdasarkan sifat-sifatnya dan komposisinya. Zat dapat diidentifikasi dari sifat fisikanya. Contoh sifat fisika adalah warna, titik leleh, dan titik didih. Sifat fisika dapat diukur dan diamati tanpa mengubah komposisi atau identitas dari suatu zat. Beberapa contoh lain dirangkum dalam Tabel 1.2.
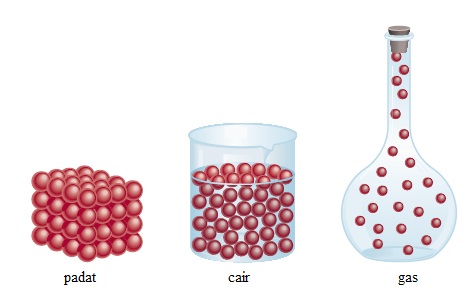
Sebagai contoh, kita dapat mengukur titik lebur es menggunakan termometer dengan memanaskan batu es, kemudian kita mencatat suhu tepat pada waktu es mencair (dikonversi menjadi air). Air (cair) berbeda dari es (padat) hanya dalam hal penampilan wujudnya, tetapi tidak berbeda dalam hal komposisinya. Jadi, perubahan es menjadi air adalah perubahan fisika. Kita dapat membekukan air untuk mengembalikannya menjadi es lagi. Oleh karena itu, titik leleh suatu zat adalah sifat fisika. Demikian pula, ketika kita mengatakan bahwa gas helium lebih ringan daripada udara, kita mengacu pada sifat fisika. Setiap kuantitas fisika dituliskan atau disimbolkan dengan huruf italic atau huruf yunani (misalnya massa disimbolkan m).
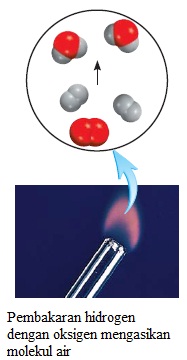
Peristiwa pembakaran gas hidrogen dengan gas oksigen menghasilkan air. Perubahan gas hidrogen dan gas oksigen menjadi komponen air menggambarkan sifat kimia. Kita mengamati sifat ini sebagai perubahan kimia, dalam hal ini pembakaran. Setelah terjadi perubahan kimia, zat kimia yang mula-mula (gas hidrogen dan gas oksigen) yang habis bereaksi akan menghasilkan zat kimia air yang berbeda dari hidrogen ataupun oksigen. Kita tidak bisa mengembalikan hidrogen dan oksigen dari air dengan cara perubahan fisika, seperti mendidihkan atau membekukan.
Setiap kali kita merebus telur, kita telah membuat perubahan kimia. Ketika berada pada suhu sekitar 100°C, kuning telur dan putih telur mengalami perubahan, yang berubah tidak hanya penampilan fisikanya, tetapi susunan kimiawinya juga. Ketika dimakan, telur berubah lagi oleh zat di dalam tubuh kita yang disebut enzim. Peristiwa pencernaan ini adalah contoh lain dari perubahan kimia. Peristiwa yang terjadi selama proses pencernaan tergantung pada sifat kimia dari enzim dan makanan.
Semua sifat materi yang dapat diukur dikelompokkan menjadi dua kategori tambahan, yaitu: sifat ekstensif dan sifat intensif. Nilai yang diukur dari sifat ekstensif tergantung pada seberapa banyak materi yang diukur. Sebagai contoh massa, yang merupakan kuantitas materi dalam sampel yang diberikan dari suatu zat adalah sifat ekstensif. Lebih banyak jumlah materi berarti bertambah massanya. Nilai dari sifat ekstensif yang sama dapat ditambahkan bersama-sama. Sebagai contoh, dua keping tembaga akan memiliki massa gabungan yang adalah jumlah massa masing-masing keping tersebut. Panjang dua lapangan tenis adalah jumlah dari panjang masing-masing lapangan tenis. Volume dapat didefisikan sebagai panjang kali lebar kali tinggi sebuah dadu merupakan sifat ekstensif. Nilai dari suatu kuantitas sifat ekstensif tergantung pada jumlah materi (bersifat aditif). Jadi, massa, panjang dan volume adalah contoh sifat ekstensif.
Nilai yang diukur dari sifat intensif tidak tergantung pada seberapa banyak materi yang diukur. Contoh sifat intensif adalah densitas (kepadatan atau kerapatan), sering juga disebut rapat jenis, yang didefinisikan sebagai massa suatu benda dibagi dengan volumenya. Temperatur juga termasuk contoh sifat intensif. Misalkan kita memiliki dua gelas air pada suhu yang sama, jika kita menggabungkan keduanya untuk membuat kuantitas tunggal air dalam gelas besar, suhu kuantitas air yang lebih besar yang digabung ini akan sama seperti pada kedua gelas terpisah tadi. Massa, panjang, volume dan sifat ekstensif lainnya bersifat aditif, sedangkan kerapatan, suhu dan sifat intensif lainnya tidak bersifat aditif.
Tabel 1.2 Contoh Sifat Fisika dan Sifat Kimia
Sifat Fisika
|
Sifat Kimia
|
|
Suhu
|
Jumlah
|
Karat (pada besi)
|
Warna
|
Bau dan Rasa
|
Pembakaran (minyak bumi)
|
Titik lebur
|
Kelarutan
|
Memudar/noda (pada perak)
|
Titik didih
|
Kekerasan
|
Mengeras (pada semen)
|
Konduktivitas kelistrikan
|
||