Asam dan basa sama akrabnya dengan aspirin dan susu magnesium hanya saja sebagian besar orang tidak tahu nama kimianya — asam asetilsalisilat (aspirin) dan magnesium hidroksida (susu magnesium). Selain menjadi bahan dasar dari banyak produk obat dan rumah tangga, kimia asam-basa penting dalam proses industri dan penting dalam mempertahankan sistem biologis. Sebelum kita membahas reaksi asam-basa, kita perlu tahu lebih banyak tentang asam dan basa itu sendiri.
Sifat Umum Asam dan Basa
Dalam Bagian 2.7 kita mendefinisikan asam sebagai zat yang terionisasi dalam air menghasilkan ion H⁺ dan basa sebagai zat yang terionisasi dalam air menghasilkan ion OH⁻. Definisi ini dirumuskan pada akhir abad kesembilan belas oleh ahli kimia Swedia Svante Arrhenius untuk mengelompokkan zat yang sifatnya sudah diketahui ketika larut dalam air.
Asam
- Asam memiliki rasa asam; misalnya, cuka berasa asam mengandung asam asetat, lemon dan buah jeruk lainnya mengandung asam sitrat.
- Asam menyebabkan perubahan warna indikator asam-basa; misalnya, asam mengubah warna lakmus dari biru menjadi merah.
- Asam bereaksi dengan logam tertentu, seperti seng, magnesium, dan besi, menghasilkan gas hidrogen. Reaksi khas adalah antara asam klorida dan magnesium:
- Asam bereaksi dengan karbonat dan bikarbonat, seperti Na₂CO₃, CaCO₃, dan NaHCO₃, menghasilkan gas karbon dioksida (Gambar 4.6). Sebagai contoh,
- Larutan asam dalam air menghantarkan arus listrik.
Basa
- Basa memiliki rasa pahit.
- Basa terasa licin; misalnya, sabun, yang mengandung basa, menunjukkan sifat ini.
- Basa menyebabkan perubahan warna indikator asam-basa; misalnya, basa mengubah warna lakmus dari merah menjadi biru.
- Larutan basa dalam air menghantarkan arus listrik.
Asam dan Basa Brønsted
Definisi asam dan basa Arrhenius terbatas karena hanya berlaku untuk larutan dalam air. Definisi yang lebih luas diusulkan oleh ahli kimia Denmark Johannes Brønsted pada tahun 1932; asam Brønsted adalah donor proton, dan basa Brønsted adalah akseptor proton. Perhatikan bahwa definisi Brønsted tidak memerlukan asam dan basa pada larutan dalam air. Asam hidroklorat adalah asam Brønsted karena ia menyumbangkan proton dalam air:
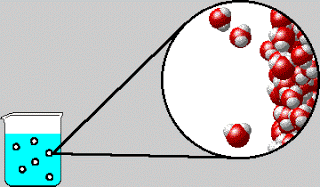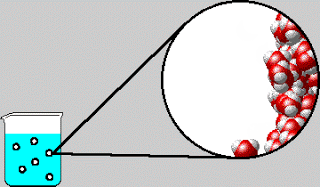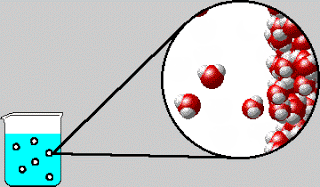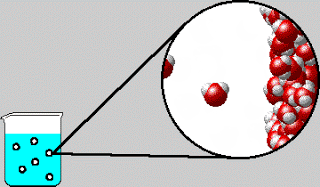
Perhatikan bahwa ion H⁺ adalah atom hidrogen yang kehilangan elektronnya; H⁺ adalah proton yang tanpa elektron dan neutron. Ukuran proton adalah sekitar 10⁻¹⁵ m, dibandingkan dengan diameter untuk atom atau ion rata-ratanya sekitar 10⁻¹⁰ m. Partikel bermuatan positif yang sangat kecil ini tidak dapat eksis sebagai entitas terpisah dalam larutan karena daya tarik yang kuat terhadap kutub negatif (atom O) dalam H₂O. Akibatnya, proton ada dalam bentuk terhidrasi seperti yang ditunjukkan pada Gambar 4.7. Oleh karena itu, ionisasi asam klorida harus ditulis sebagai berikut:
Proton terhidrasi, H₃O⁺, disebut ion hidronium. Persamaan ini menunjukkan reaksi di mana asam Brønsted (HCl) menyumbangkan proton ke basa Brønsted (H₂O).
Eksperimen menunjukkan bahwa ion hidronium terhidrasi lebih lanjut sehingga proton dapat memiliki beberapa molekul air yang tertarik dengannya. Karena sifat asam proton tidak terpengaruh oleh tingkat hidrasi, dalam diskusi ini kita akan terbiasa menggunakan H⁺ (aq) untuk mewakili proton terhidrasi. Notasi ini untuk kenyamanan, tetapi H₃O⁺ lebih dekat dengan fakta eksperimen. Perlu diingat bahwa kedua notasi tersebut mewakili spesi yang sama dalam larutan berair.
Asam yang biasa digunakan di laboratorium meliputi asam hidroklorat (HCl), asam nitrat (HNO₃), asam asetat (CH₃COOH), asam sulfat (H₂SO₄), dan asam fosfat (H₃PO₄). Tiga asam pertama adalah asam monoprotik; yaitu, setiap satuan asam menghasilkan satu ion hidrogen setelah ionisasi:
Seperti disebutkan sebelumnya, karena ionisasi asam asetat tidak seluruhnya (perhatikan panah ganda), asam itu adalah elektrolit yang lemah. Untuk alasan ini disebut asam lemah (lihat Tabel 4.1). Di sisi lain, HCl dan HNO₃ adalah asam kuat karena keduanya adalah elektrolit kuat, sehingga keduanya terionisasi seluruhnya dalam larutan (perhatikan penggunaan panah tunggal).
Asam sulfat (H₂SO₄) adalah asam diprotik karena setiap satuan asam melepaskan dua ion H⁺, dalam dua langkah terpisah:
H₂SO₄ adalah elektrolit kuat atau asam kuat (langkah pertama ionisasi seluruhnya), tetapi HSO₄⁻ adalah asam lemah atau elektrolit lemah, dan kita membutuhkan panah ganda untuk merepresentasi ionisasi yang tidak seluruhnya.
Asam triprotik, yang menghasilkan tiga ion H⁺, jumlahnya relatif sedikit. Asam triprotik yang paling terkenal adalah asam fosfat, yang ionisasinya
Ketiga spesi (H₃PO₄, H₂PO₄⁻, dan HPO₄²⁻) dalam contoh ini adalah asam lemah, dan kita menggunakan panah ganda untuk merepresentasi setiap langkah ionisasi. Anion seperti H₂PO₄⁻ dan HPO₄²⁻ ditemukan dalam larutan fosfat berair seperti NaH₂PO₄ dan Na₂HPO₄. Tabel 4.3 mencantumkan beberapa asam kuat dan lemah yang umum.
Tabel 4.3 Beberapa Asam Kuat dan
Asam Lemah Yang Umum
Gambar 4.8 Ionisasi amonia dalam air membentuk ion amonium dan ion hidroksida.
Tabel 4.1 menunjukkan bahwa natrium hidroksida (NaOH) dan barium hidroksida [Ba(OH)₂] adalah elektrolit yang kuat. Ini berarti bahwa keduanya seluruhnya terionisasi dalam larutan:
Ion OH⁻ dapat menerima proton sebagai berikut:
H⁺(aq) + OH⁻(aq) → H₂O(l)
Dengan demikian, OH⁻ adalah basa Brønsted.
Ammonia (NH₃) diklasifikasikan sebagai basa Brønsted karena dapat menerima ion H⁺ (Gambar 4.8):
NH₃(aq) + H₂O(l) ⇋ NH₄⁺(aq) + OH⁻(aq)
Amonia adalah elektrolit yang lemah (dan karenanya basa lemah) karena hanya sebagian kecil molekul NH₃ terlarut yang bereaksi dengan air membentuk ion NH₄⁺ dan OH⁻.
Basa kuat yang paling umum digunakan di laboratorium adalah natrium hidroksida. Basa itu murah dan mudah larut. (Faktanya, semua hidroksida logam alkali larut dalam air). Basa lemah yang paling umum digunakan adalah larutan amonia berair, yang kadang-kadang keliru disebut ammonium hidroksida. Tidak ada bukti bahwa spesi NH₄OH sebenarnya ada selain ion NH₄⁺ dan OH⁻ dalam larutan. Semua unsur Golongan 2A membentuk hidroksida tipe M(OH)₂, di mana M menunjukkan logam alkali tanah. Dari hidroksida ini, hanya Ba(OH)₂ yang larut dalam air. Magnesium dan kalsium hidroksida digunakan dalam kedokteran dan industri. Hidroksida dari logam lain, seperti Al(OH)₃ dan Zn(OH)₂ tidak larut dalam air dan tidak digunakan sebagai basa.
Contoh 4.3 mengklasifikasikan zat sebagai asam Brønsted atau basa Brønsted.
Contoh 4.3
Klasifikasi masing-masing spesi berikut dalam larutan air sebagai asam atau basa Brønsted: (a) HBr, (b) NO₂⁻, (c) HCO₃⁻.
Strategi
Apa karakteristik asam Brønsted? Apakah asam Brønsted mengandung setidaknya satu atom H? Dengan pengecualian amonia, sebagian besar basa Brønsted yang akan kita jumpai pada tahap ini adalah anion.
Penyelesaian
(a) Kita tahu bahwa HCl adalah asam. Karena Br dan Cl keduanya adalah halogen (Golongan 7A), kita harapkan HBr, seperti HCl, terionisasi dalam air sebagai berikut:
HBr(aq) → H⁺(aq) + Br⁻(aq)
Oleh karena itu HBr adalah asam Brønsted.
(b) Dalam larutan, ion nitrit dapat menerima proton dari air membentuk asam nitrit:
NO₂⁻(aq) + H⁺(aq) → HNO₂(aq)
Sifat ini menjadikan NO₂⁻ basa Brønsted.
(c) Ion bikarbonat adalah asam Brønsted karena terionisasi dalam larutan sebagai berikut:
HCO₃⁻ (aq) ⇋ H⁺(aq) + CO₃²⁻(aq)
Ion ini juga merupakan basa Brønsted karena dapat menerima proton membentuk asam karbonat:
HCO₃⁻(aq) + H⁺(aq) ⇋ H₂CO₃(aq)
Komentar
Spesi HCO₃⁻ dikatakan bersifat amfoter karena memiliki sifat asam dan sifat basa. Panah ganda menunjukkan bahwa ini adalah reaksi yang dapat balik.
Latihan
Klasifikasi masing-masing spesi berikut sebagai asam atau basa Brønsted: (a) SO₄²⁻, (b) HI.
Reaksi Netralisasi Asam-Basa
Reaksi netralisasi adalah reaksi antara asam dan basa. Umumnya, reaksi larutan asam-basa berair menghasilkan garam dan air, yang merupakan senyawa ionik yang terdiri dari kation selain H⁺ dan anion selain OH⁻ atau O²⁻:
asam + basa → garam + air
Zat yang kita kenal sebagai garam meja atau garam dapur (NaCl) adalah produk dari reaksi asam-basa
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
Namun, karena asam dan basa adalah elektrolit yang kuat, keduanya sepenuhnya terionisasi dalam larutan berair. Persamaan ioniknya adalah
H⁺(aq) + Cl⁻(aq) + Na⁺(aq) + OH⁻(aq) → Na⁺(aq) + Cl⁻(aq) + H₂O(l)
Oleh karena itu, reaksi dapat direpresentasi oleh persamaan ion bersih
H⁺(aq) + OH⁻(aq) → H₂O(l)
Baik Na⁺ maupun Cl⁻ adalah ion spektator.
Jika kita memulai reaksi sebelumnya dengan jumlah molar yang sama dari asam kuat dan basa kuat, pada akhir reaksi kita hanya akan memiliki garam dan tanpa sisa asam atau basa. Rekasi ini adalah karakteristik dari reaksi netralisasi asam-basa.
Reaksi antara asam lemah seperti asam hidrosianat (HCN) dan basa kuat adalah
HCN(aq) + NaOH(aq) → NaCN(aq) + H₂O(l)
Karena HCN adalah asam lemah, HCN tidak terionisasi dalam larutan. Jadi, persamaan ionik ditulis sebagai
HCN(aq) + Na⁺(aq) + OH⁻(aq) → Na⁺(aq) + CN⁻(aq) + H₂O(l)
dan persamaan ion bersihnya adalah
HCN(aq) + OH⁻(aq) → CN⁻(aq) + H₂O(l)
Perlu dicatat bahwa hanya Na⁺ merupakan ion spektator, OH⁻ dan CN⁻ bukan.
Berikut ini juga contoh reaksi netralisasi asam-basa, yang diwakili oleh persamaan molekul:
Persamaan yang terakhir terlihat berbeda karena tidak menunjukkan adanya air sebagai produk. Namun, jika kita menyatakan NH₃(aq) sebagai NH₄⁺(aq) dan OH⁻(aq), seperti yang dibahas sebelumnya, maka persamaannya menjadi
HNO₃(aq) + NH₄⁺(aq) + OH⁻(aq) → NH₄NO₃(aq) + H₂O(l)
Reaksi Asam-Basa Yang Membentuk Gas
Garam tertentu seperti karbonat (mengandung ion CO₃²⁻), bikarbonat (mengandung ion HCO₃⁻), sulfit (mengandung ion SO₃²⁻), dan sulfida (mengandung ion S²⁻) bereaksi dengan asam membentuk produk gas. Sebagai contoh, persamaan molekul untuk reaksi antara natrium karbonat (Na₂CO₃) dan HCl(aq) adalah (lihat Gambar 4.6)
Na₂CO₃(aq) + 2HCl(aq) → 2NaCl(aq) + H₂CO₃(aq)
Asam karbonat tidak stabil dan jika ada dalam larutan dalam konsentrasi yang cukup akan terurai sebagai berikut:
H₂CO₃(aq) → H₂O(l) + CO₂(g)
Reaksi serupa yang melibatkan garam lain yang disebutkan adalah
Ulasan Konsep
Manakah dari diagram berikut yang paling merepresentasi asam lemah? Yang merupakan asam yang sangat lemah? Yang merupakan asam kuat? Proton ada dalam air sebagai ion hidronium. Semua asam bersifat monoprotik. (Untuk penyederhanaan, molekul air tidak diperlihatkan.)